|
作者:1°C
2019年03月28日,国家药品监督管理局、国家卫生与健康委员会组织有关专家研究论证,遴选出了第二批临床急需境外新药,为落实国务院常务会议有关会议精神,加快临床急需的境外上市新药进入中国。
2018年以来,国家药品监督管理局深入优化临床急需境外新药审评审批,佳达修9,欧迪沃,可瑞达,Soliris (依库珠单抗)等一批创新药加速进入中国,本文重点分析国家局发布的第二批临床急需境外新药,并同时简单更新第一批名单中药物中国开发进展。
一、政策助力:全球创新药物加速进入中国
近年,国家局推出多项重要的审评审批政策,如优先审评、接受药品境外临床试验数据、优化进口创新药审评程序、临床默示许可等等,系列政策给全球创新药加速进入中国提供了前所未有的机遇,这其中,罕见病药物更是受益颇多,罕见病药物在中国上市的机会难得一遇。
此次,第二批临床急需境外新药名单有一个明显特点:罕见病药物比例占一半,第二批名单中15款药物为罕见病用药,如β-半乳糖苷酶A缺乏的治疗药物Fabrazyme(Agalsidase Beta);除此外,有多款药物以"较上市产品有治疗优势"纳入名单中,如丙肝药物Maviret,艾滋病药物Biktarvy。
第2批临床急需境外新药中,尚有多个值得关注的点,具体的:
1. 多个药物国内已上市 药物凭借单适应症进入名单
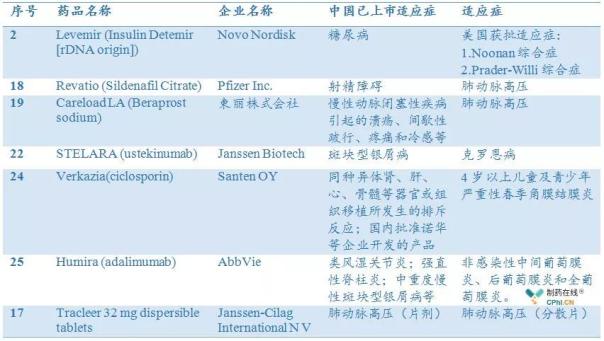
根据笔者所查询到的信息,第二批名单中药品已在国内上市,药物凭借某单适应症进入名单,例如地特胰岛素用于Noonan 综合症,乌司奴单抗用于克罗恩病,阿达木单抗用于葡萄膜炎,Santen开发的贝前列素新适应症角膜结膜炎。
另外,爱可泰隆波生坦分散片同样进入名单,根据笔者查询到的信息波生坦片已在国内上市,药物凭借新的剂型进入。
这些药物进入第2批临床急需名单后,其后续的特定的新适应症拓展或是新剂型获批将会进一步加速。
2. 名单中5款药物处于上市申请阶段
除上文提到的已上市药物外,有5款药物已向NMPA递交上市申请,这其中包括两款罕见病药物,即法布雷病治疗药物阿加糖酶α/β,以及3款具有明显治疗优势的药物如,丙肝直接抗病毒 药物Maviret,艾滋病药物Biktarvy,PCSK9单抗Praluent(Alirocumab)。
这其中,Mavyret 将会进一步增加丙肝患者治疗选择,其治疗周期减少(唯一一款疗程为8周的DAA药物)、治疗费用大幅降低,为同类最优产品。
艾滋病药物Biktarvy则是吉利德推出的一款整合酶抑制剂类完整方案单一片剂药物,是目前美国一线用药,而国内艾滋病用药依旧十分落后,固定剂量复方缺乏,疗效优异的整合酶抑制剂产品更是罕见,医保对固定剂量复方或完整方案单一片剂药物覆盖极差,该款药物上市将会大大提高国内艾滋病药物的可及性,改善患者用药。
|