|
作者:邴绍昌/赵琨
近年来国内医药市场正在经历巨大变革,尤其是仿制药企业市场格局,从最初“同品种药品通过一致性评价的生产企业达到3家以上的,在药品集中采购等方面不再选用未通过一致性评价的品种”,到“凡2007年10月1日前批准上市的列入国家基本药物目录(2012年版)中的化学药品仿制药口服固体制剂(附件),原则上应在2018年底前完成一致性评价”,再到“化学药品新注册分类实施前批准上市的含基本药物品种在内的仿制药,自首家品种通过一致性评价后,其他药品生产企业的相同品种原则上应在3年内完成一致性评价。逾期未完成的,企业经评估认为属于临床必需、市场短缺品种的,可向所在地省级药品监管部门提出延期评价申请,经省级药品监管部门会同卫生行政部门组织研究认定后,可予适当延期。逾期再未完成的,不予再注册”。国内仿制药市场的敲门砖多了项一致性评价,再就是要靠质量与价格杀进集中采购,抑或是去争取集中采购之外的市场份额。
那么在一致性评价政策出台三年以后,国内仿制药在临床试验资源有限的情况下厮杀已达到何种程度?
说临床之前,还是先看下目前已通过一致性评价或者视同通过一致性评价(按化药新注册分类批准的仿制药)的品种。截至2018年底,苯磺酸氨氯地平已有5家企业通过一致性评价,包括黄河、扬子江、华润赛科、东瑞和京新;瑞舒伐他汀已经有京新、正大天晴、海正和先声4家通过;阿莫西林胶囊同样有4家,包括联邦、康恩贝、石药中诺和科伦;蒙脱石散有维奥、先声、扬子江和宏济堂通过一致性评价;恩替卡韦两个剂型均有4家企业通过,其中胶囊剂有正大天晴、青峰、海思和广生堂,分散片剂有正大天晴、青峰、东瑞、贝克;而目前已经超过3家通过一致性评价的品种也已经超过11个。
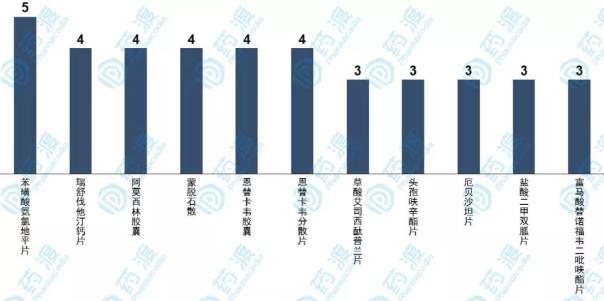
图1 一致性评价通过企业数TOP10品种
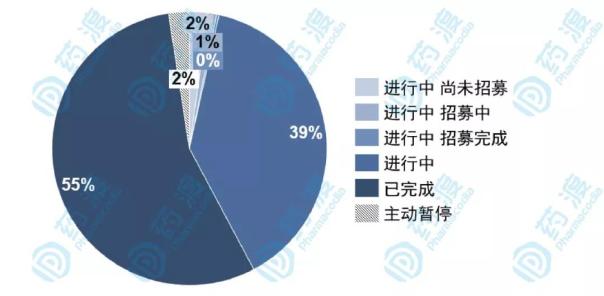
图2 2013-2019年生物等效性试验状态分布
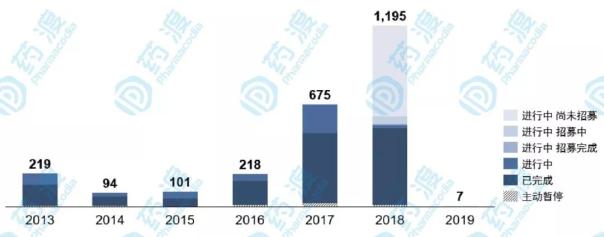
图3 2013-2019年生物等效性试验公示数量及状态
在CDE网站收录的国内生物等效性临床中,总数量已经达到2,507个,占平台登记总数量的24.4%,开展数量在2015年后迅速翻倍增长。生物等效性试验数量最多的药品为盐酸二甲双胍,目前已经有85个临床登记号,其中52个临床已完成,31个进行中;第二位为苯磺酸氨氯地平,共有64个临床受理号,其中完成数量超过2/3;第三位为阿莫西林,目前共有53个受理号,约六成已完成临床研究。
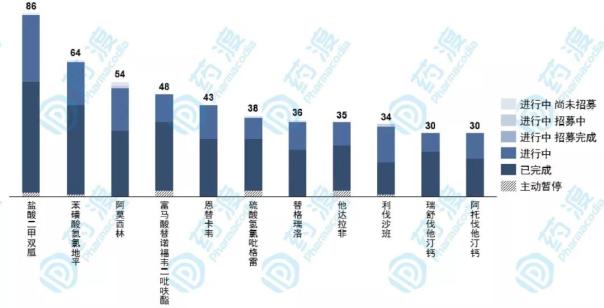
图4 生物等效性试验公示数量TOP10品种及状态
|