|
文 | 滴水司南
2020年01月10日,为深化"放管服"改革,简化申报材料,优化办事流程,强化风险防控,提高药品再注册审批工作效率,根据《药品管理法》《药品注册管理办法》有关要求,本着"标准不降低,流程可优化"的原则,江苏省药品监督管理局官网发布《江苏省药品再注册申报指南》,这是2019年12月1日起实施史上"最严"的《药品管理法》后首个省药监局发布的再注册申报指南,为药品生产企业再注册申报提供了具有可操作性的指南,本文对药品再注册有关政策内容进行了分析。

一、药品再注册制度过往今昔
根据我国《药品注册管理办法》相关规定,药品批准文号的有效期为5年,有效期届满继续生产的,申请人应当在有效期届满前6个月申请再注册,其实从2002年12月1日实施的《药品注册管理办法》(试行)(局令第35号)开始,药品再注册的定义也在发生着变化。

二、新监管时代,从严再注册受理
在落实"放管服"方面,简化申报材料,优化办事流程,强化风险防控,提高药品再注册审批工作效率,减少了企业负担,但也从严管理不再再注册情形。
不再再注册情形对照表


三、再注册申报资料有哪些



四、再注册需要多少费用
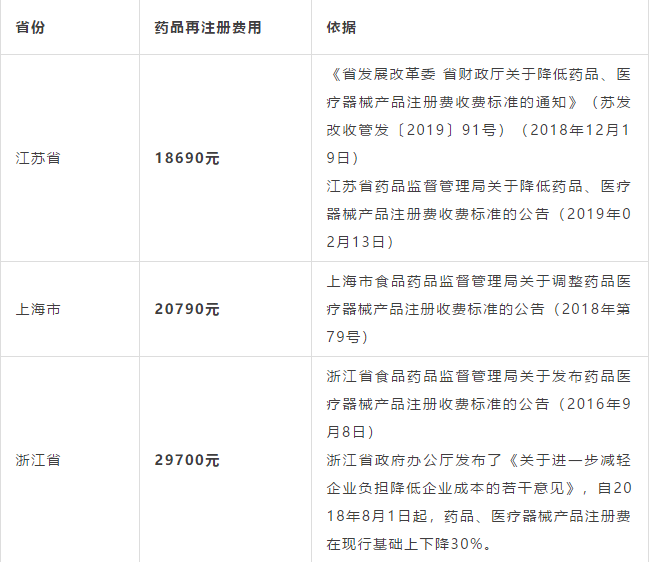
2020年,进入新监管时代,是不平凡之年,在落实"放管服"方面,相信各省药监局将持续简化药品再注册申报材料,优化办事流程,提高药品再注册审批工作效率,减少企业负担,但会从严管理不再再注册情形,药品再注册不再"走过场",如常年未生产的品种再恢复生产时,须向省级食品药品监督管理部门提出和产现场检查申请,通过现场检查且产品检验合格后,方可上市销售未提出申请的品种及5年内未生产的品种不予再注册,保批准文号(常年未生产的品种)后续不知还要投入多少?建议药品上市许可持有人提前布局清理好批准文号的调整工作,对企业产品结构进行合理优化,相信药品再注册制度必将有力促进医药生产的健康发展。
|