|
1类化药临床审批概况
2019年4月,共有17个中国1类化药获得国家药品监督管理局(NMPA)的临床试验默示许可,具体信息如下表所示:
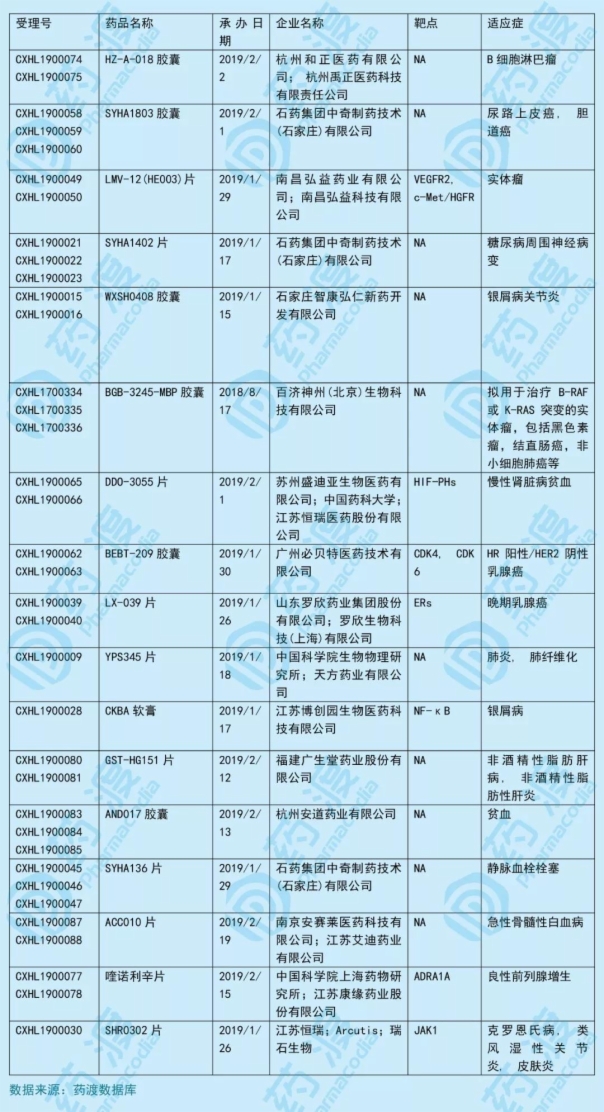
1.HZ-A-018
HZ-A-018由杭州和正医药有限公司和杭州禹正医药科技有限责任公司联合研发,拟用于治疗B细胞淋巴瘤。2019年2月,国家药品监督管理局(NMPA,原CFDA)受理本品的临床试验申请(化药1类)。2019年4月,被默认许可临床试验。
目前用于治疗B细胞淋巴瘤的中国1类药物如下表所示:
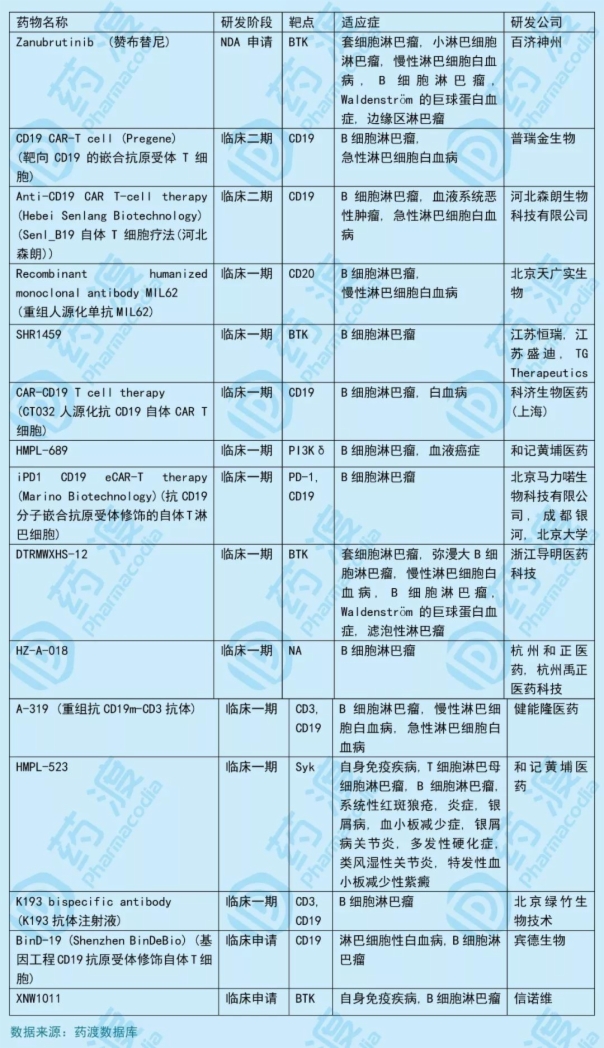
2.SYHA1803
SYHA1803由石药集团中奇制药技术(石家庄)有限公司研发,拟用于治疗肝内胆管癌、尿路上皮细胞癌。2019年2月,国家药品监督管理局(NMPA,原CFDA)受理本品的临床试验申请(化药1类)。2019年4月,被默认许可临床试验。该产品临床前研究显示具有优异的体外酶、细胞活性及体内抗肿瘤效果,以及良好的安全性和药代动力学特点。
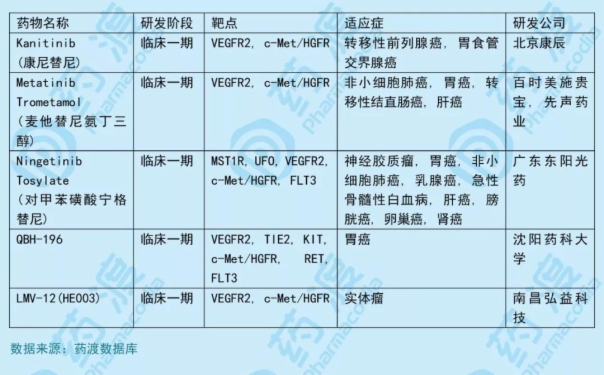
3.LMV-12(HE003)
LMV-12(HE003) 是由南昌弘益药业有限公司(南昌弘益科技有限公司子公司)自主研发、具有自主知识产权的首个c-Met、VEGFR2多靶点抗肿瘤创新药物。2019年2月,国家药品监督管理局(NMPA,原CFDA)受理本品的临床试验申请(化药1类),2019年4月,获得临床试验默示许可。
目前靶向c-Met、VEGFR2的中国1类同靶点药物如下表所示:
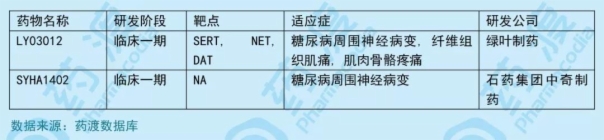
4.SYHA1402
SYHA1402由石药集团中奇制药技术(石家庄)有限公司研发,拟用于治疗糖尿病周围神经病变。2019年1月,国家药品监督管理局(NMPA,原CFDA)受理本品的临床试验申请(化药1类),2019年4月,获得临床试验默示许可。临床前研究显示,该产品通过逆转疾病病理变化而达到保护神经细胞作用,具有优异的体内疗效,同时具有良好的安全性和药代动力学特点,极有希望在临床研究中展现出良好的糖尿病神经病变治疗效果。
目前用于治疗糖尿病周围神经病变的中国1类药物如下表所示:
5.WXSH0408
WXSH0408由石家庄智康弘仁新药开发有限公司研发,拟用于治疗银屑病关节炎。2019年1月,国家药品监督管理局(NMPA,原CFDA)受理本品的临床试验申请(化药1类),2019年4月,获得临床试验默示许可。
|